 Infectología
Infectología
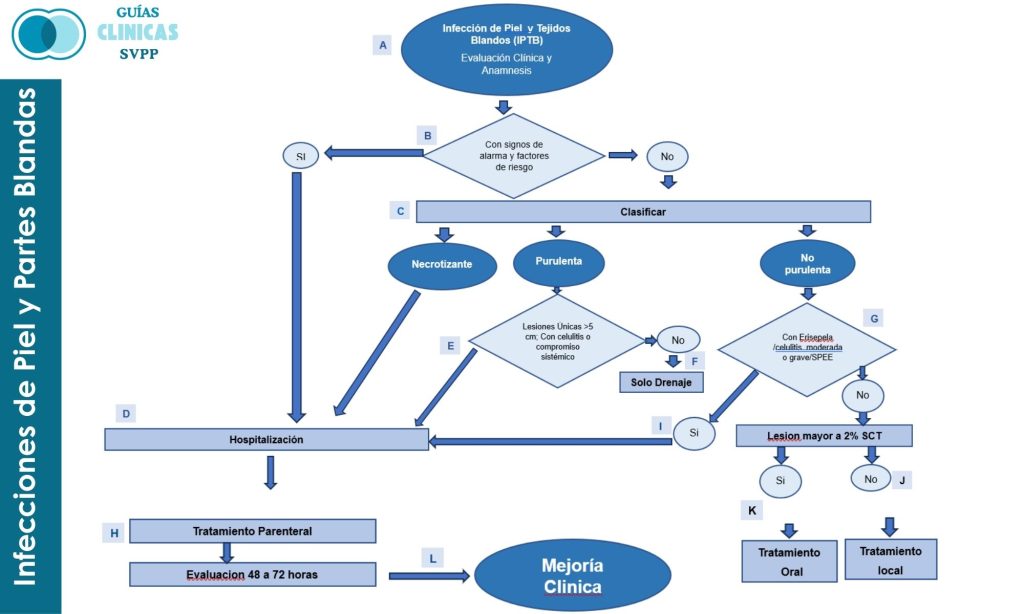
Infecciones de piel y partes blandas
Evaluación Clínica y Anamnesis
Se excluye la población neonatal debido a consideraciones especiales.
- Evaluar el estado general y la lesión.
- Recopilar información sobre el estado inmunológico del paciente, comorbilidades (p. ej., diabetes, desnutrición, VIH), historial de traumatismos o mordeduras, exposiciones (p. ej., agua dulce o salada), higiene deficitaria, y uso previo de antibióticos.
- Considerar la edad como factor predisponente (p. ej., impétigo más frecuente en menores de 5 años; tetraciclinas solo en mayores de 8 años).
Signos de alarma y factores de riesgo
- Compromiso sistémico (fiebre >38°C o <36°C, taquicardia >90 lpm, taquipnea >24 rpm, alteración de la conciencia, hipotensión, disfunción orgánica).
- Dolor intenso desproporcionado a los hallazgos físicos.
- Progresión rápida del cuadro clínico.
- Presencia de bulas hemorrágicas, equimosis o necrosis cutánea.
- Edema o induración de la piel que se extiende más allá del eritema.
- Crepitación palpable (presencia de gas en los tejidos).
- Hipoestesia localizada en la piel.
- Absceso de gran tamaño (mayores de 3 cm en pacientes de 6 a 11 meses, >4 cm en 1 a 8 años, >5 cm en mayores de 8 años).
- Lactantes menores de 3 meses).
- Inmunosupresión (p. ej., quimioterapia activa, neutropenia, VIH con CD4 <200, cáncer activo, uso de corticoides o inmunosupresores).
- Comorbilidades descontroladas (p. ej., diabetes, insuficiencia renal/hepática, enfermedad vascular, asplenia, neuropatía).
- Extensión mayor al 9% del área corporal total.
- Compromiso de áreas de riesgo (mano o cabeza).
- Celulitis periorbitaria.
Clasificar
- IPTB No Purulenta: Impétigo, Ectima, Erisipela, Celulitis, Sindrome de Piel Escaldada(SPEE)
- Impétigo: es una infección superficial de la piel, muy común en la infancia, especialmente en climas cálidos y húmedos, frecuente en preescolares, clima cálido, higiene deficiente y lesiones cutáneas preexistentes (ej. escabiosis, muy prevalente en algunas comunidades de Venezuela) aumentan el riesgo (2). Se clasifica en dos formas principales: ampollar que responde en un 70% de los casos a Staphylococcus aureus productor de exotoxina y costrosa o mielecerica, forma más frecuente (Streptococcus pyogenes y/o Staphylococcus aureus). (II-A) (3).
- Celulitis: proceso infeccioso de la dermis y tejido celular subcutáneo, dinámico, caracterizado por dibujar placas eritematosas de bordes mal definidos, dolorosas, calientes, con o sin presencia de adenopatías regionales y eventualmente con manifestaciones sistémicas como fiebre y malestar general, dependiendo de la severidad y extensión del cuadro. (I-A) (4). Staphylococcus aureus resulta ser el agente etiológico más frecuente, también están involucrados Streptococcus pyogenes, BGN, entre otros. La prevalencia de S. aureus resistente a la meticilina adquirido en la comunidad (SARM-AC) como causa de IPTB es un desafío global y local y su frecuencia va en franco ascenso (I-A) (1, 6).
- Erisipela: infección bacteriana aguda de la piel que afecta a la dermis superior y se extiende de manera importante hacia los vasos linfáticos superficiales. Se caracteriza por un eritema cutáneo indurado, de bordes bien definidos y elevados, que la distingue de la celulitis, que afecta a tejidos más profundos (19). Aunque puede ocurrir a cualquier edad, presenta particularidades clínicas y epidemiológicas en pediatría que requieren un diagnóstico y manejo precisos para evitar complicaciones. Se considera una forma específica y superficial de celulitis (I-A) (20). Mayoritariamente el Streptococcus pyogenes es el agente etiológico de esta noxa, mas no el único.
- Síndrome de la Piel Escaldada Estafilocócica (SPEE): observa con mayor frecuencia en niños menores de cinco años de edad, y la mayoría de los casos ocurren entre los 2 y 3 años, centrada su patogénesis en la escisión de la desmogleína-1 mediada por exotoxinas del Staphylococcus aureus, lo que provoca ruptura de las uniones densas y descamación intraepidérmica. (15) Topológicamente muy parecido al Impétigo ampollar, pero, este responde a la liberación local de estas toxinas, por lo que a menudo se presenta con hallazgos cutáneos localizados. Por el contrario, el SPEE se debe a la propagación sistémica de estas toxinas, lo que provoca lesiones cutáneas generalizada y un cuadro clínico grave. (15).
- IPTB Purulenta: Absceso cutáneo, Forúnculo, Ántrax.
- Absceso Cutáneo: aun cuando cualquiera de los agentes implicados en las IPTB pudiera generarlo, es el Staphylococcus aureus el principal patógeno involucrado en la génesis de esta noxa. En Venezuela se ha reportado alta prevalencia de SARM-AC, con clones relacionados a los circulantes en la región (7, 8, 11).
- IPTB Necrosante: Fascitis Necrosante, Piomiositis.
- Fascitis Necrosante: Se caracteriza por la friabilidad de la fascia superficial, un exudado grisáceo y la ausencia notable de pus, provocan una destrucción tisular generalizada que puede extenderse desde la epidermis hasta la musculatura profunda. (12-14). La fascitis necrosante se distingue principalmente por su causa: polimicrobiana o tipo I, involucra microorganismos aeróbicos y anaeróbicos, gran positivos y negativos o monomicrobiana o tipo II, generada principalmente por Streptococcus pyogenes (tipo II) (12). El signo cardinal es un dolor desproporcionado a los hallazgos cutáneos, la fascitis necrosante debe considerarse en pacientes con manifestaciones sistémicas de sepsis, como taquicardia, leucocitosis, acidosis o hiperglucemia marcada y manifestación clínica de IPTB. (12-14)
- La penetración bacteriana en los compartimentos fasciales de la cabeza y el cuello puede provocar angina de Ludwig. La infección de tipo I a menudo se asocia con la presencia de gas en el tejido, por lo que es difícil distinguirla de la gangrena gaseosa. La gangrena de Fournier comienza de forma abrupta con un dolor intenso y puede propagarse rápidamente desde la región perineal hasta la pared abdominal anterior, los músculos de los glúteos y, en el caso de los varones, los genitales. (12-14)
- En aproximadamente el 50% de los pacientes con fascitis necrosante causada por Estreptococo del grupo A, la infección se inicia en la profundidad de los tejidos blandos, sin una puerta de entrada, a menudo en sitios de traumatismo no penetrante (distensión muscular o hematoma). (12-13)
- Es una emergencia quirúrgica absoluta, la exploración quirúrgica es el estándar de oro para el diagnóstico y tratamiento. No se debe retrasar la cirugía por estudios de imagen (II-A). (12, 13)
- Piomiositis: el Staphylococcus aureus es en un 90% de los casos responsable directo de la patología, incluyendo SARM-AC (I-A) (17,18).
- Clínicamente se caracteriza por fiebre, cojera dolorosa y dolor localizado en pelvis, extremidades inferiores, tronco y columna, como áreas más frecuentemente afectadas y Iliopsoas, musculatura obturatriz y musculatura glútea los grupos musculares más comúnmente afectados y los preescolares y escolares los grupos etarios mas afectados. (IV-A) (17,18). Aunque considerada «tropical», se reportan casos en todo el mundo. (17)
Hospitalización
- Manejo de sepsis si es necesario.
- Estudios Diagnósticos:
- Hematología completa, PCR, Hemocultivos (pacientes inmunocomprometidos, sepsis, mala evolución con tratamiento empírico, presentaciones atípicas, sospecha de gérmenes atípicos), cultivo de secreción en lesiones purulentas.
- Estudio de Imágenes: ecografía o resonancia magnética si se sospecha de infección profunda u osteomuscular.
Antibióticos sistémicos y drenaje
- Celulitis extensa asociada al absceso.
- Síntomas sistémicos (SIRS, Hipotensión)
- Inmunosupresión
- Absceso de gran tamaño (referencia por edad: >3 cm en 6-11 meses, >4 cm en 1-8 años, >5 cm en mayores de 8 años).
- Falla terapéutica o recurrencia después del I&D.
- Sospecha o confirmación de bacteriemia (siempre con agente bactericida).
- Empírico (cubrir SAMR):
- Ambulatorio (5-7 días): Oral (TMP-SMX o Clindamicina). Linezolid oral como alternativa
- Hospitalario (7-14 días): Intravenoso (Vancomicina)
- Alternativas IV: Linezolid, Daptomicina, Clindamicina (IV), Tigeciclina o Ceftarolina (consultar con especialista).
- Para infección grave con SIRS/hipotensión (cubrir SAMR y SAMS con efecto bactericida): Vancomicina + Oxacilina. (Clindamicina y TMP-SMX son bacteriostáticos y no se recomiendan como monoterapia si hay sospecha de bacteriemia).
Drenaje
- Lesiones Pequeñas (forunculosis): Tratamiento local (limpieza con clorhexidina), no se sugiere antibiótico sistémico.
- Lesiones Únicas <5 cm (sin celulitis ni compromiso sistémico): Drenaje puede ser suficiente.
- Forúnculos Grandes (>2 cm), Carbunclos, Abscesos, Quiste Epidermoide Infectado:Insicion y Drenaje I&D.
- Se recomienda añadir antibióticos adyuvantes, según sensibilidad local, para mejorar las tasas de curación (I-A).
- El envío de material para cultivo y antibiograma es crucial en el para vigilar la flora microbiológica causal y su resistencia. (III-C) (6, 10).
Ambulatorio
- Paciente estable, sin signos sistémicos de infección.
- Lesión localizada y no extensa (<2% del área total de la superficie corporal para impétigo; para otras IPTB <9% del área corporal total).
- Ausencia de factores de riesgo significativos para complicaciones.
- Buena adherencia esperada al tratamiento y red de apoyo social adecuada.
Tratamiento endovenoso
- Fascitis Necrosante :
- Manejo de Emergencia:
- Sospecha Alta: Consulta Quirúrgica Urgente, reanimación hemodinámica intensiva y Desbridamiento Quirúrgico
- Antibióticos Empíricos Intravenosos (Amplio Espectro): Debe cubrir Gram positivos (incluyendo SAMR), Gram negativos (incluyendo Pseudomonas aeruginosa) y anaerobios.
- Régimen: Vancomicina (o Linezolid si hay falla renal) + Cefepime (o Piperacilina/Tazobactam) + Clindamicina.
- Clindamicina: Adición recomendada por su efecto inhibidor de toxinas (especialmente en infecciones por pyogenes o S. aureus mediadas por toxinas y shock tóxico).
- Ajuste: Una vez se disponga de aislamiento microbiológico, ajustar la terapia a un espectro más estrecho.
- Piomiositis:
- Etiología Principal: aureus (90%, incluyendo SAMR), S. pyogenes, bacilos Gram negativos.
- Tratamiento Empírico Inicial IV: Vancomicina (o Linezolid en pacientes con falla renal).
- Para Piomiositis por SAMS: Cefazolina u Oxacilina.
- Cobertura de Gram Negativos: Añadir solo en pacientes inmunosuprimidos o con trauma penetrante muscular.
- Drenaje Temprano: Si hay formación de abscesos.
- Duración: 2 a 6 semanas, ajustada según la evolución clínica y la gravedad.
- Control: Realizar imágenes de control en pacientes con bacteriemia persistente para identificar focos no drenados.
Celulitis/Erisipela Moderada o Grave
- Celulitis/Erisipela Moderada ( con síntomas sistémicos)
- Tratamiento Intravenoso (IV): Cefazolina o Oxacilina (cubrir SAMS y Streptococcus spp.).
- Terapia Secuencial Oral: Cefadroxilo una vez resueltos los síntomas sistémicos.
- Duración: 5 días (extender si no hay mejoría).
- Celulitis/Erisipela Grave (sepsis, disfunción orgánica, inmunosuprimidos, factores de riesgo para Gram negativos):
- Tratamiento IV Empírico:
- La Vancomicina continúa siendo droga de elección (I-A) (6,10,11). Factores de Riesgo para Gram Negativos (p. ej., heridas por inmersión, úlceras por presión, infección hospitalaria, inmunosupresión, infección necrosante): Considerar adicionar cobertura de amplio espectro (p. ej., cefalosporina de tercera/cuarta generación o carbapenémico).
- Alternativas a Vancomicina/Clindamicina (para SAMR): Daptomicina (no usar si hay compromiso pulmonar) o Ceftarolina.
- Terapia Secuencial Oral (después de 48h de antibióticos IV activos contra SAMR y resolución de síntomas): TMP-SMX o Clindamicina (si resistencia local <10%).
- Duración: 5 días (extender si no mejora).
- Sospecha de SAMR (p. ej., infección/colonización previa por SAMR, trauma penetrante, uso de drogas IV, celulitis abscedadas, inmunosupresión, falla terapéutica):
- Tratamiento Antibiótico: Incluir un antimicrobiano efectivo contra SAMR y estreptococos. (Estudios no muestran beneficio de cobertura empírica de SAMR en celulitis leve en áreas de alta prevalencia).
Tratamiento Oral
- Múltiples Lesiones Extenso o Brotes de Glomerulonefritis Post-estreptocócica:
- Manejo de Soporte: Elevación del área afectada y manejo de factores predisponentes (p. ej., edema, dermatosis subyacentes).
- Si hay falla al tratamiento o falta de soporte para seguimiento, considerar hospitalizacion
- Impétigo (ampolloso y no ampolloso):
- Agentes Etiológicos Comunes: Staphylococcus aureus y Streptococcus pyogenes.
- Cobertura de SAMR (Staphylococcus aureus Resistente a Meticilina): Considerar si la prevalencia local es >10-15% o si existen factores de riesgo. Factores de Riesgo para SAMR: Infección o colonización previa por SAMR, trauma penetrante, uso de drogas intravenosas, celulitis abscedadas, inmunosupresión, falla terapéutica con terapia de primera línea sin cobertura SAMR.
- Duración del Tratamiento: Generalmente 5-10 días, extendiendo si no hay mejoría clínica.
- Sospecha/Confirmación SAMS o Streptococcus spp.: Cefalosposina de primera o segunda generación, Amoxicilina-Ac. Clavulanico. Penicilina oral si solo S. pyogenes). Cefadroxilo preferida por perfil de seguridad y palatabilidad en pediatría.
- Sospecha/Confirmación SAMR: Clindamicina (si resistencia local <10%) o Trimetoprim-sulfametoxazol (TMP-SMX). (TMP-SMX limitado si se sospecha S. pyogenes por falta de cobertura).
- Factores de Riesgo para SAMR: Infección o colonización previa por SAMR, trauma penetrante, celulitis abscedadas, inmunosupresión, falla terapéutica con terapia de primera línea sin cobertura SAMR.
- Celulitis/Erisipela Leve (sin signos sistémicos):
- Etiología Común: S. pyogenes (principal en erisipela) y S. aureus (principal en celulitis, incluyendo SAMS y SAMR).
- Tratamiento Oral: Cefalosporina de primera generación (p. ej., Cefadroxilo).
- Duración del Tratamiento: Generalmente 5-10 días, extendiendo si no hay mejoría clínica.
- No debe perderse el foco sobre el SAMR-AC frecuente en el País, por tanto, la combinación de Clindamicina y Trimetropin-Sulfametoxazol resulta otra opción manejable en base a la data microbiológica local
- Ectima:
- Siempre Tratamiento Oral: Mismas consideraciones que el impétigo extenso
Tratamiento Local
- Agentes Etiológicos Comunes: Staphylococcus aureus y Streptococcus pyogenes. El tratamiento empírico debe cubrirlos.
- Impétigo (ampolloso y no ampolloso):
Tratamiento Tópico(<2% SCT): Mupirocina o Ácido Fusídico (2-3 veces al día por 5-7 días).
Evaluación a las 48 horas
- Mejoría Clínica:
- Considerar desescalar el antibiótico (según cultivos si disponibles).
- Rotar de terapia intravenosa a oral, si el paciente tolera la vía oral y sus comorbilidades están controladas.
- Considerar alta temprana o manejo ambulatorio domiciliario si se cumplen los criterios.
- No Mejoría Clínica:
- Reevaluar el diagnóstico inicial.
- Buscar complicaciones (p. ej., abscesos no drenados, infección profunda).
- Ajustar el tratamiento antibiótico (escalar espectro o cambiar de agente, basado en cultivos si disponibles).
- Considerar procedimientos quirúrgicos adicionales.
- Si hay bacteriemia persistente, buscar focos no drenados y realizar ecocardiograma para descartar siembras (p. ej., endocarditis).
Autores
Aquad, Roque (1), Franco, José Vicente (2), Morillo Gimon, Lourdes (3), Valera Aracelis (4)
- Infectologo pediatra, Clínica Lugo Maracay (2) Infectologo pediatra ULA, Profesor universitario ULA., (3) Infectologo pediatra Hospital de niños JM de los Ríos , Colaborador docente Postgrado Universitario Hospital de Niños JM de los Ríos, (4) Infectologo pediatra Hospital General Nacional Dr. Ángel Larralde.
Nombre autor responsable: Lourdes Morillo Gimon Correo: lougimon07 gmail.com
BIBLIOGRAFÍA
- Guía de práctica clínica colombiana para el tratamiento de infecciones bacterianas de piel y tejidos blandos superficiales en Población pediátrica: Gutiérrez-Tobar, I.F., et al (2023). Guía de práctica clínica colombiana para el tratamiento de infecciones bacterianas de piel y tejidos blandos superficiales en Población pediátrica. Infectio, 27(2), 114-131.
- Infecciones de piel y partes blandas (Marín Cruz I, Carrasco Colom J): Marín Cruz, I., & Carrasco Colom, J. (2023). Infecciones de piel y partes blandas. Protoc diagn ter pediatr, 2, 271-283.
- Infecciones Bacterianas de Piel y Tejidos Blandos – Síntesis de Conocimientos: Guinez, J. (2016). Infecciones Bacterianas De Piel Y Tejidos Blandos. Síntesis de Conocimientos, Departamento de Educación en Ciencias de la Salud, Facultad de Medicina, Universidad de Chile. Publicado el 28 de octubre de 2016.
- Practice Guidelines for the Diagnosis and Management of Skin and Soft Tissue Infections: 2014 Update by the Infectious Diseases Society of America (IDSA): Stevens, D. L., Bisno, A. L., Chambers, H. F., Dellinger, E. P., Goldstein, E. J. C., Gorbach, S. L., et al. (2014). Practice Guidelines for the Diagnosis and Management of Skin and Soft Tissue Infections: 2014 Update by the Infectious Diseases Society of America. Clinical Infectious Diseases, 59(2), e10-52. doi:10.1093/cid/ciu296.
- Algoritmo de manejo ambulatorio de infecciones de piel y tejidos blandos de la comunidad Parte 1: Supuradas y no supuradas: Barcelona, L., Musante, R., Alonso, L., Rodríguez Iantorno, P., Guidetto, B., & Laserre, N. (s.f.). Algoritmo de manejo ambulatorio de infecciones de piel y tejidos blandos de la comunidad Parte 1: Supuradas y no supuradas. Ministerio de Salud de la Nación, Argentina.
- Guía de Práctica Clínica para el Diagnóstico y Manejo de las Infecciones de Piel y Tejidos Blandos en Colombia: Valderrama-Beltrán, et al (2019). Guía de Práctica Clínica para el Diagnóstico y Manejo de las Infecciones de Piel y Tejidos Blandos en Colombia. Infectio, 23(4), 318-346.
- Astorga F, Escobar J, Gil R, Pérez-Alfonzo R, Sifontes S, Lindo E, et al. Etiología y sensibilidad bacteriana en pacientes con infecciones de piel y partes blandas en un centro de referencia de Caracas, Venezuela. Rev Panam Infectol. 2008;10(4):24-31. [Consultado 7 Jul 2025]
- Brindle R, Williams I, Barton E, Featherstone P. Assessment and management of patients with skin and soft tissue infections in the UK. Clin. Pract. 2021, 11, 65–74. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC7931029/ [Consultado 7 Jul 2025]
- Stevens DL, Bryant AE. Necrotizing Soft-Tissue Infections. N Engl J Med. 2017 Dec 7;377(23):2253-2265. Disponible en: https://www.nejm.org/doi/full/10.1056/NEJMra1600673 [Consultado 9 Jul 2025]
- Sharma P, Karthik N, Badkur M, et al. (June 30, 2025) Clinical Profile and Outcomes of Patients With Necrotizing Soft Tissue Infections: A Prospective Observational Study. Cureus 17(6): e87035. Disponible en: https://www.cureus.com/articles/368421-clinical-profile-and-outcomes-of-patients-with-necrotizing-soft-tissue-infections-a-prospective-observational-study#!/ [Consultado 9 Jul 2025]
- Cruickshank M, Hart J. Staphylococcal Scalded Skin Syndrome. [Updated 2024 May 19]. En: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK534158/ [Consultado 10 Jul 2025]
- Vij N, Ranade AS, Kang P, Belthur MV. Primary Bacterial Pyomyositis in Children: A Systematic Review. J Pediatr Orthop. 2021 Oct 1;41(9): e849-e854. Disponible en: https://pubmed.ncbi.nlm.nih.gov/34411048/ [Consultado 12 Jul 2025]
- Verma, Sanjay. (2016). Pyomyositis in Children. Current Infectious Disease Reports. 18.10.1007/s11908-016-0520-2. Disponible en: https://www.researchgate.net/publication/294730488_Pyomyositis_in_Children/citation/download [Consultado 10 Jul 2025]
- Taha, I., Tadmori, I., Kojmane, W. y Hida, M. (2023) Erisipela en niños: Factores de riesgo y manejo en urgencias pediátricas. Open Journal of Pediatrics , 13 , 914-920. Disponible en: https://www.scirp.org/journal/paperinformation?paperid=129094 [Consultado 14 Jul 2025]
- Brazel M, Desai A, Are A, Motaparthi K. Síndrome de piel escaldada estafilocócica e impétigo ampolloso. Medicina (Kaunas). 24 de octubre de 2021; 57 (11) Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC8623226/ [Consultado 10 Jul 2025]
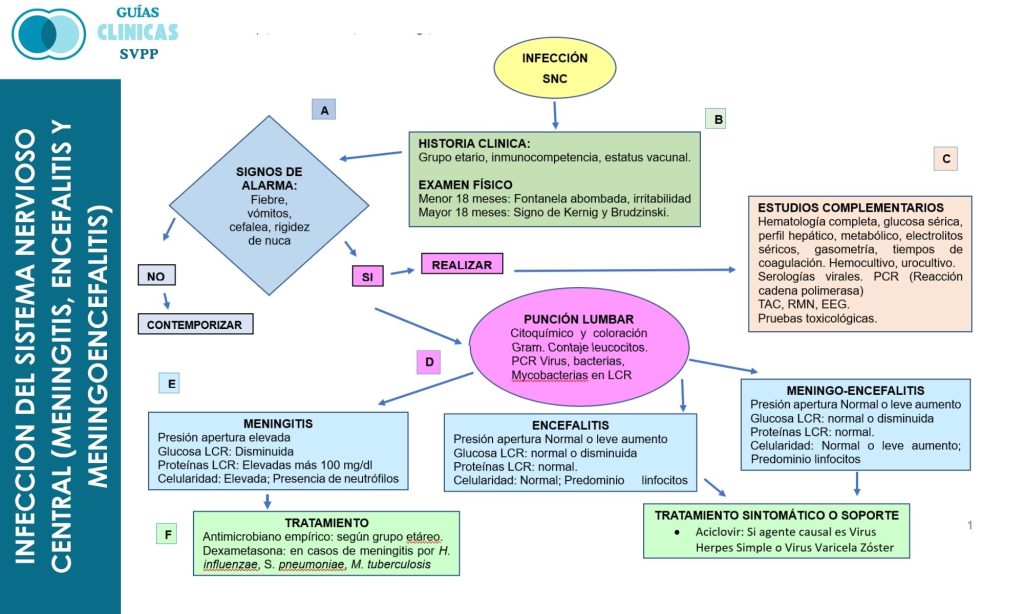
Infección del Sistema Nervioso Central (Meningitis, Encefalitis y Meningoencefalitis)
Etiología
Se habla de meningitis cuando existe inflamación de las meninges, y encefalitis cuando la inflamación afecta el parénquima cerebral, siendo la etiología de estas infecciones variable involucrando infecciones por virus, bacterias, hongos y micobacterias según grupo etario o estado inmune del paciente, así como diversas causas no infecciosas.(1)
Las infecciones del Sistema Nervioso Central (SNC) son más frecuentes en la población pediátrica que en adultos, principalmente en menores de cinco años. Dentro de las diferentes formas de meningitis adquiridas en la comunidad, la enfermedad bacteriana es asociada con la mayor morbimortalidad a nivel mundial. Los patógenos que causan meningitis bacteriana dependen de la edad, estado inmune y la presencia de factores de riesgo concurrentes, estas suponen el 5% de las meningitis. (1–4)

Hallazgos Clínicos
Las manifestaciones clínicas en ocasiones pueden ser inespecíficas, generalmente, la meningitis aguda se caracteriza por rápida aparición de fiebre, rigidez de nuca, cefalea, fotofobia y/o alteración del estado de conciencia. La tríada clásica de fiebre, cefalea y rigidez de nuca nos debe hacer pensar en meningitis bacteriana. Pueden presentarse otros síntomas como: malestar general, fatiga, náuseas y/o vómitos. Ante la presencia de convulsiones, déficits neurológicos focales o parálisis de pares craneales debemos pensar en meningoencefalitis. Al examen físico pueden estar presentes los signos de irritación meníngea de Brudzinski y Kernig, aunque en menores de 18 meses es difícil la evaluación de estos.
La rigidez de nuca y la cefalea son difíciles de identificar en lactantes, pero se puede observar fontanela abultada, además de fiebre o hipotermia, letargo o irritabilidad, rechazo del alimento, llanto anormal, continuo, débil o agudo, signos de dificultad respiratoria y convulsiones.
Algunos pacientes pueden desarrollar síntomas y signos de aumento de la presión intracraneal, secundario a edema cerebral, hidrocefalia o una lesión ocupante de espacio. La complicación más grave de la hipertensión intracraneal es la hernia cerebral. En casos graves, puede producirse, sepsis, shock séptico, fallo multiorgánico o coagulación intravascular diseminada (CID).
Diagnóstico
Ante la sospecha de neuro infección, se debe realizar una historia clínica detallada, examen físico, análisis de sangre y punción lumbar (PL) antes de iniciar el tratamiento. La base diagnóstica es el estudio del LCR. Algunos hallazgos clínicos como erupción cutánea, lesiones cutáneas específicas, herpangina, conjuntivitis, faringitis, vómitos y diarrea pueden sugerir etiología viral. Sugieren encefalitis signos de focalización, datos epidemiológicos como contacto con garrapatas, mosquitos y roedores, o enfermos en brotes estacionales de meningoencefalitis.
En casos fulminantes con hipotensión e insuficiencia orgánica, la toma de hemocultivo seguida de la administración de antibióticos puede preceder a la anamnesis completa, la exploración física y la punción lumbar.
Estudios complementarios
Por lo general en las meningitis bacterianas existe leucocitosis con predominio de neutrófilos siendo la leucopenia de mal pronóstico y un valor de procalcitonina (PCT) >0.5 ng/mL el predictor más fuerte en sangre. Orientan más hacia meningitis viral: leucocitosis con predominio de linfocitos y proteína C Reactiva negativa con alto valor predictivo negativo.
Punción lumbar
A menos que esté contraindicado, en cualquier paciente con sospecha de infección del SNC, se debe realizar una punción lumbar, tan pronto como sea posible, ante la sospecha de etiología bacteriana debe realizarse antes del inicio del tratamiento antibiótico. (2)
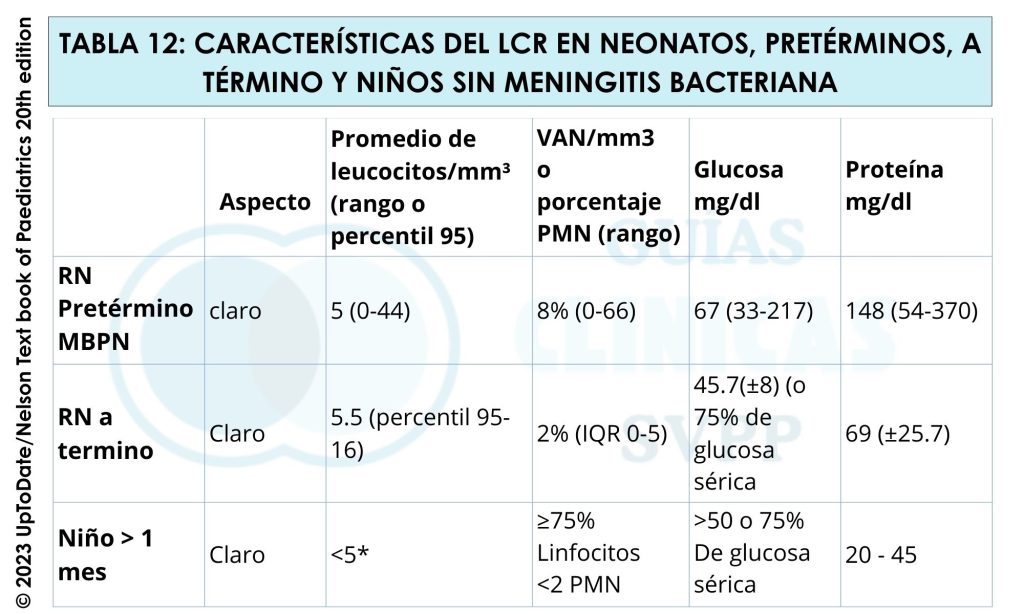
a Citoquímico: celularidad, concentración de glucosa, proteínas y lactato. El lactato: se considera sugestivo de MB cuando es > 3,8 mmol/l, en meningitis asépticas suele ser < 2 mmol/l (1,4,5).
b Constituyen el gold estándar en el diagnóstico de meningitis bacteriana. Puede ser negativo para la tinción gram y el cultivo tan solo 2-4 horas después de administración de antibiótico.
c Pueden ser negativos si se inicia antibióticos antes de la toma de muestras, el traslado y preservación de la muestra es inadecuado y en caso de VHS cuando se realiza antes de 72 horas de los síntomas ó 5-7 días de tratamiento antiviral y ante la presencia de sangre contaminante en la muestra. Es especialmente útil cuando no hay aislamiento en el cultivo o para patógenos virales. Existen paneles con los agentes bacterianos y virales más comunes.
d Ante sospecha de infección fúngica del SNC de tipo absceso o lesión ocupante de espacio (ej. histoplasmoma): realizar TAC cerebral o RMC para localizar la lesión, biopsia del área sospechosa, evaluación histopatológica directa y cultivo de tejido. Cuando esto no es posible, son útiles la sospecha por clínica, epidemiología, factores del huésped, y otros exámenes de laboratorio. Pueden ser de ayuda exámenes moleculares del LCR y β-d-glucano galactomanano sérico.
e Se debe sospechar de meningoencefalitis por amebas de vida libre por Naegleria spp. ante antecedentes de inmersión en agua dulce y Acanthamoeba spp. o Balamuthia spp. en pacientes inmunodeprimidos.
*Aunque muy poco frecuente, la meningoencefalitis puede deberse a una infección por helmintos como Angiostrongilus cantonensis y cursa con eosinofilia.
* Los retrasos en el análisis de laboratorio del LCR pueden alterar el recuento celular como resultado de la lisis en el LCR. Se observa una reducción progresiva tanto de neutrófilos como de linfocitos después de 4 horas.
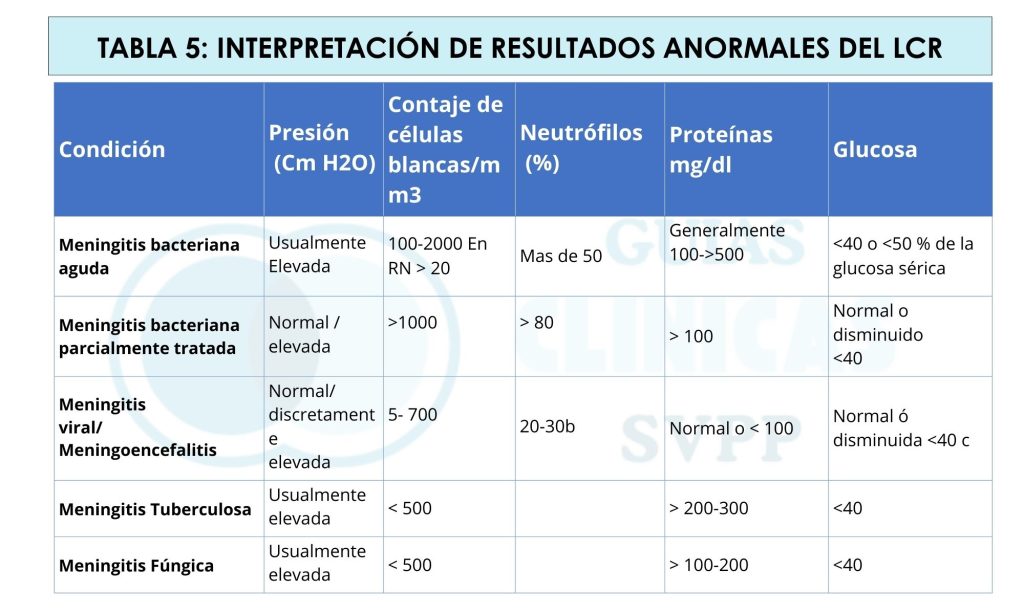 a Algunas infecciones por neumococo o meningococo pueden cursar con < 500 células, adicionalmente esto puede verse en pacientes con signos de shock séptico o inmunodeprimidos y en fases iniciales de la infección.
a Algunas infecciones por neumococo o meningococo pueden cursar con < 500 células, adicionalmente esto puede verse en pacientes con signos de shock séptico o inmunodeprimidos y en fases iniciales de la infección.
b Puede haber pleocitosis > 1 000 células/μl en el 10% y predominio de neutrófilos en el 20-30%, especialmente en fases iniciales de la infección.
c En infecciones por herpesvirus o virus de la parotiditis. (1)
*Se han descrito casos de meningitis por enterovirus y parechovirus sin pleocitosis en lactantes pequeños.(1, 4)
*La citoquímica del LCR no se afecta hasta varios días después de iniciar el tratamiento en MB (1)
*ADA ; > 8 UI/l es sugestivo de meningitis tuberculosa.
*En encefalitis por Herpes simple puede haber elevación de la glucorraquia.(4)
*En Meningitis bacteriana en inmunodeprimido, el número de leucocitos puede ser < 100
* En Meningitis bacteriana parcialmente tratada pueden predominar mononucleares si el tratamiento es prolongado
* en meningitis tuberculosa y en la fúngica pueden predominar PMN inicialmente, luego son los mononucleares los que predominan la mayor parte del tiempo.
* Las convulsiones no aumentan el recuento de células del LCR.
Complicaciones de la Punción lumbar: cefalea, infección, sangrado, dolor de espalda, dolor radicular, hipotensión intracraneal y neumoencéfalo. Otra complicación poco frecuente es la herniación cerebral en presencia de aumento de la presión intracraneal. (2)
CONTRAINDICACIÓN PARA LA PUNCIÓN LUMBAR
a papiledema, disminución del nivel de consciencia, pupilas desiguales, dilatadas o poco reactivas, respiración irregular, postura de decorticación o descerebración
b Se realizan las medidas terapéuticas y las pruebas adecuadas antes de la punción lumbar
c CID y recuento de plaquetas <50000/mm³): corrección adecuada primero. Uso de anticoagulante. ¿Se pueden suspender temporalmente? La antiagregación plaquetaria no la contraindica. Frente a Coagulopatía (corrección previa)
d Imagenología en caso de sospecha de médula anclada. Guía del procedimiento de punción lumbar mediante fluoroscopia, ecografía o TC. (realizada por Neurocirugia)
Punción traumática (con sangre)
La interpretación más segura de una punción traumática es contar el número total de glóbulos blancos e ignorar el recuento de glóbulos rojos. Si hay más glóbulos blancos que el rango normal para la edad, la opción más segura es el tratamiento. Algunas guías sugieren que, en las punciones traumáticas, el recuento de glóbulos blancos y proteínas puede corregirse con base en el siguiente cálculo: 1 glóbulo blanco por cada 500-700 glóbulos rojos y 0,01 g/L de proteína por cada 1000 glóbulos rojos. Sin embargo, esto no es fiable. (z) También se puede usar la siguiente formula:
Leucocitos reales en LCR = leucocitos totales en LCR – leucocitos contaminantes
Leucocitos contaminantes= (hematíes LCR × leucocitos en sangre)/hematíes en sangre
*Considere la posibilidad de una hemorragia subaracnoidea cuando haya glóbulos rojos inexplicables o persistentes en el LCR.
Estudios de Imágenes cerebrales:
No se deben realizar de rutina en pacientes con sospecha de neuro infección,
pero si se encuentran los siguientes hallazgos clínicos: Puntuación de coma de Glasgow inferior a 10, signos de focalización neurológica, déficit de pares craneales, edema de papila, deterioro neurológico rápido, antecedentes de hidrocefalia, neurocirugía reciente, traumatismo craneoencefálico ó inmunodepresión grave se debe realizar neuroimagen si es fácilmente accesible, de lo contrario, se debe postponer la punción lumbar hasta la resolución de los hallazgos clínicos sin retrasar el tratamiento. (1-2)
También se recomiendan en caso de evolución no satisfactoria y para buscar complicaciones, como abscesos o trombosis.
Cuando se pospone la punción lumbar se deben recolectar muestras de sangre (incluidos hemocultivos) e iniciar el tratamiento antimicrobiano lo antes posible, antes de la obtención de imágenes craneales (1-5,7)
Las convulsiones son un hallazgo frecuente en niños febriles con sospecha de meningitis aguda, si estas son aisladas, de nueva aparición, sin signos de focalización neurológica u otro hallazgo clínico de riesgo no requieren imágenes craneales antes de la punción lumbar (2)
Un estado de inmunodepresión grave (p. ej., trasplante de órganos) justifica la postergación de la punción lumbar. Sin embargo, en pacientes con VIH y sospecha de un primer episodio de meningitis criptocócica, se recomienda la punción lumbar inmediata con medición de la presión de apertura y un análisis rápido del antígeno criptocócico como método diagnóstico de elección. (2)
Generalmente, la hidrocefalia es un signo tardío en la meningitis bacteriana debido a su evolución compleja; la hidrocefalia temprana puede indicar patología tuberculosa en caso de meningitis.
La resonancia magnética puede demostrar lesiones cerebrales focales como afectación del lóbulo temporal que sugiere enfermedad por VHS-1.
Electroencefalograma
El EEG puede ser útil en caso de sospecha de encefalitis, convulsiones o sospecha de estado epiléptico no convulsivo (EENC).
DIAGNÓSTICO DIFERENCIAL
Es importante tener en cuenta la meningitis parcialmente tratada, ya que es difícil de diagnosticar, por lo que los niños que se encuentren recibiendo algún esquema antibiótico, deben ser evaluados cuidadosamente, ya que pueden tener signos y síntomas modificados, retrasando su diagnóstico.(8)
Aunque no son consideradas como causa común de meningitis, otras enfermedades bacterianas pueden ser consideradas en el diagnóstico diferencial en personas que viven en áreas endémicas y/o tienen factores de riesgo específicos (brucelosis, leptospirosis, enfermedad de Lyme y rickettsiosis).
Otros problemas a ser considerados son:
- Absceso cerebral
- Absceso subdural/epidural
- Tumor cerebral
- Infiltración de leucemia a SNC
- Encefalopatía por metales pesados
- Encefalopatía metabólica
- Exposición a fármacos (AINES, TMP/SMX, Isoniazida, inmunoglobulinas intravenosas) o toxinas
- Intoxicación por alcohol o drogas
- Trastornos asociados a vasculitis o enfermedades autoinmunes (sarcoidosis, LES)
- Síndrome de Reye
- Traumatismo craneoencefálico
- Hemorragia intracraneal
- Síndrome hemolítico urémico
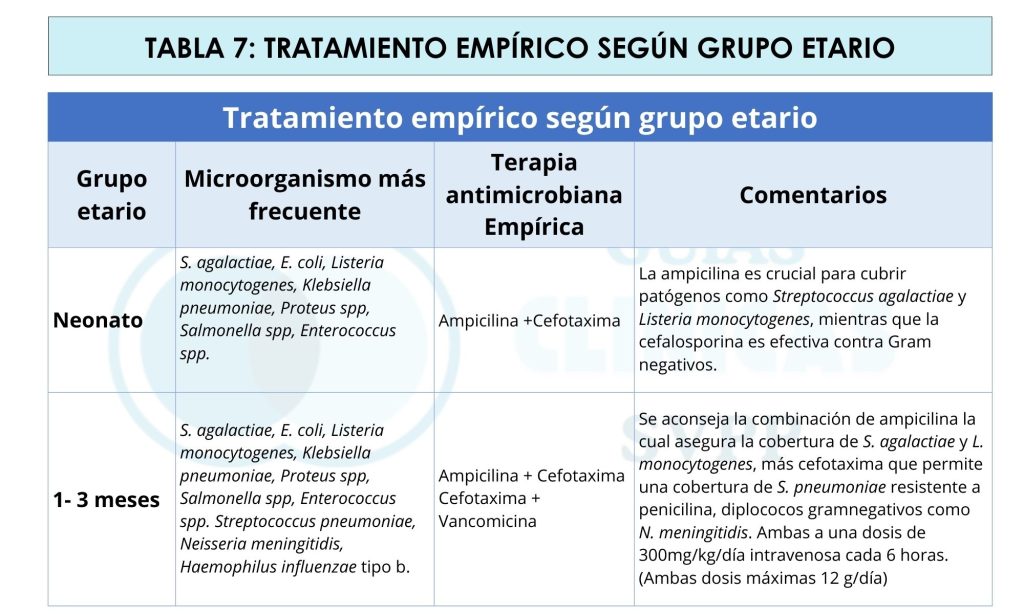
Tratamiento empíritu según grupo etario
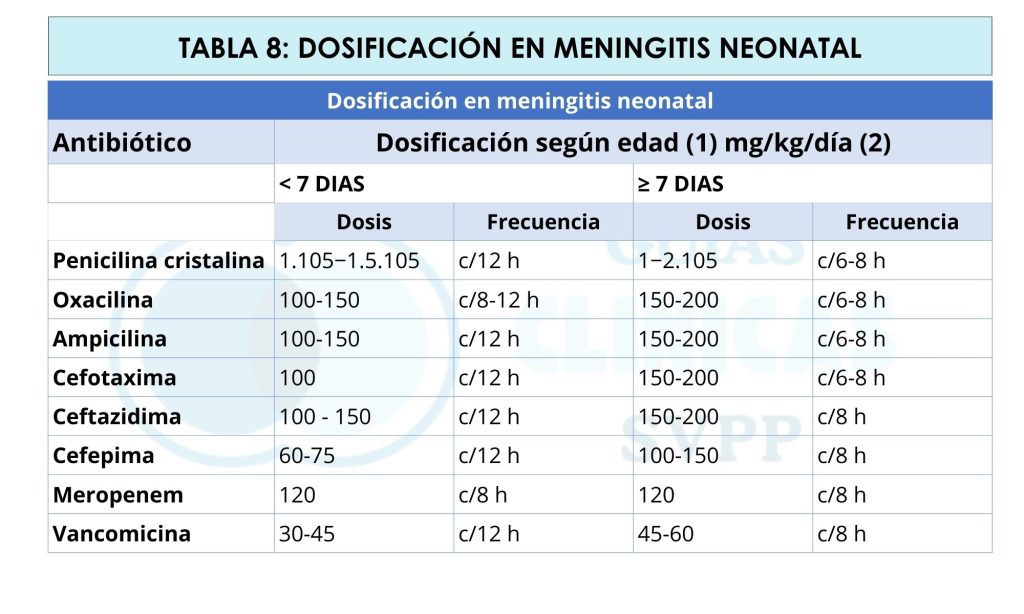
El tratamiento empírico se basa en los patógenos más probables para cada grupo de edad, considerando la epidemiología local y los patrones de resistencia. En sospecha de meningitis bacteriana neonatal el tratamiento empírico inicial recomendado se detalla en la tabla 7 y 8.
Este tratamiento se mantiene hasta que se identifique el microorganismo responsable y su sensibilidad a los antibióticos, permitiendo así ajustar la terapia a un tratamiento dirigido.
Importante: No se recomienda el uso de ceftriaxona en neonatos con hiperbilirrubinemia debido al riesgo de encefalopatía hiperbilirrubinemia, ni en los que reciben hidratación con calcio por riesgo de precipitación con el calcio intravenoso.
En meningitis por virus de herpes simple (VHS): La prontitud en el inicio de tratamiento es crucial para prevenir la morbimortalidad, aunque las indicaciones del tratamiento de forma empírica no están plenamente estandarizadas, la mayoría de especialista concuerda, en que está justificado el inicio de aciclovir.
En casos de neonatos con meningitis por Candida: Se sugiere iniciar tratamiento empírico con anfotericina B durante al menos 3 semanas, contadas a partir del primer cultivo negativo y hasta que se haya resuelto las alteraciones del LCR o anomalías radiológicas de estar presentes.
Tratamiento antimicrobiano en pacientes con meningitis bacteriana aguda de 1-3 meses de edad: Se debe iniciar de inmediato, previo a la toma de muestras para estudios microbiológicos, tinción de gram, tinta china y Ziehl-Neelsen, citoquímico y cultivo de LCR, hemocultivo. Sin embargo, no se debe retrasar el tratamiento, en caso de no tener disponibilidad o si la condición del paciente limita la toma de muestras. En este grupo etario el tratamiento estará dirigido a los microrganismos involucrados en el periodo neonatal y además se incluyen Streptococcus pneumoniae y Neisseria meningitidis. Ver tabla 7.
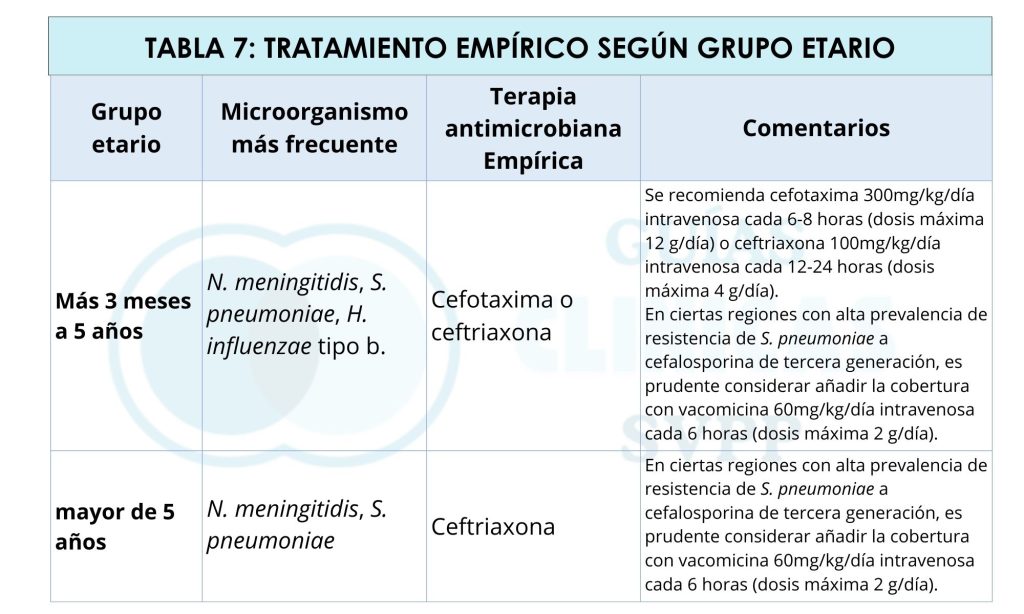
Tratamiento antimicrobiano en pacientes con meningitis bacteriana aguda de 3 meses – 5 años de edad: La terapéutica en esta edad esta fundamentalmente dirigida a Neisseria meningitidis, Streptococcus pneumoniae y en menor medida gracias a la vacunación, Haemophilus influenzae tipo b. Ver tabla 7.
Tratamiento antimicrobiano en pacientes con meningitis bacteriana aguda mayor a 5 años de edad: Para este grupo etario la etiología bacteriana más común es Neisseria meningitidis, Streptococcus pneumoniae.
- Consideraciones: al igual que los grupos de menor edad, la adición de vancomicina debe contemplarse en áreas con alta tasa de resistencia de S. pneumoniae a cefalosporina de tercera generación, se tendrá en consideración la ampicilina para cobertura de L. monocytogenes en caso de adolescentes inmunocomprometidos.
- Consideraciones: Una vez se obtengan los resultados definitivos de los cultivos y antibiograma, o reacción en cadena de polimerasa (PCR) procederemos a ajustar la terapia antibiótica de manera específica según el microorganismo identificados y su perfil de susceptibilidad.
Duración de tratamiento antimicrobiano: La duración de la terapia antimicrobiana depende del microorganismo causante y de la evolución clínica del paciente. Para la meningitis bacteriana aguda no complicada, se sugieren los periodos de tratamiento detallados en la tabla 9 de la guía. Asimismo, es importante considerar otros hallazgos paraclínicos para el manejo. Para estas consideraciones, ver la información en la tabla 10.
Tratamiento de meningitis aguda por otras etiologías: El abordaje de la meningitis fuera del periodo neonatal debe ser rápido y específico. Ante la sospecha de etiología viral por VHS, se debe iniciar de inmediato la terapia con aciclovir intravenoso. La dosis es de 60 mg/kg/día, dividida cada 8 horas para menores de 12 años, y de 30 mg/kg/día para mayores de esta edad. La duración es de 14 a 21 días.
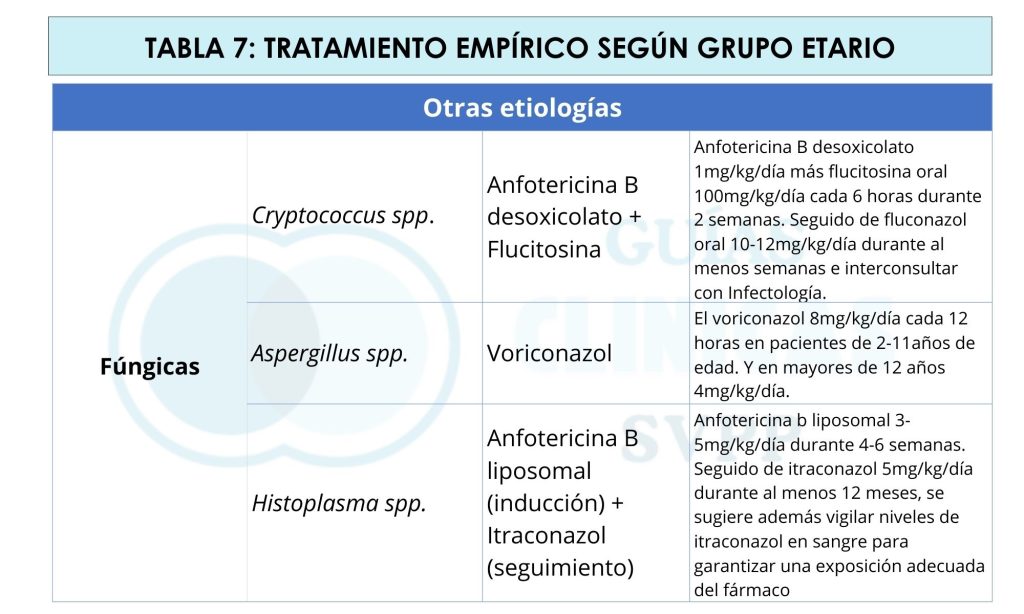
Para las etiologías fúngicas, el tratamiento es más complejo y depende del microorganismo, se utiliza anfotericina B con flucitosina para Candidiasis y Criptococosis, mientras que el voriconazol es la primera línea para la Aspergilosis. En casos de Histoplasmosis, la anfotericina B liposomal es la elección inicial, seguida de itraconazol. La evaluación continua de la evolución clínica y los parámetros del LCR es esencial. Ver tabla 7
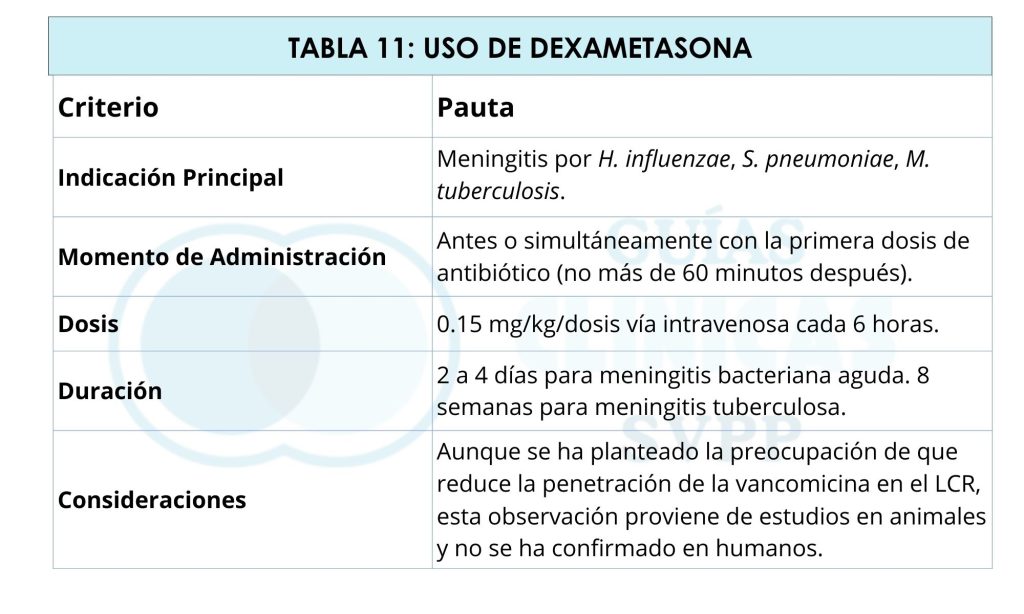
Uso de Dexametasona como tratamiento adyuvante en meningitis: La dexametasona es una terapia adyuvante que ha demostrado ser beneficiosa en la reducción de secuelas neurológicas, especialmente la hipoacusia neurosensorial, en casos de meningitis por H. influenzae tipo b, S. pneumoniae, M. tuberculosis. Actúa atenuando la respuesta inflamatoria en el espacio subaracnoideo, disminuyendo la liberación de citoquinas y mediadores inflamatorios que contribuyen al daño neuronal y edema cerebral, no obstante, es fundamental tener claro que en neonatología esta indicación no se recomienda, dado que no ha tenido beneficios demostrables. En la tabla 11, se resume las pautas clave para su administración.
Anexo
En la coloración de GRAM, la presencia de:
- Diplococos grampositivos sugieren infección neumocócica.
- Diplococos gramnegativos sugieren infección meningocócica.
- Cocobacilos gramnegativos son compatibles con infección por H. influenzae.
- Bacilos o cocobacilos grampositivos sugieren infección por Listeria. (1)
cocos grampositivos de cadena corta (Streptoccocus agalactiae) o bacilos gramnegativos (Escherichia coli). La observación de levaduras indica meningitis por Cryptococcus neoformans/gattii (levaduras encapsuladas en la tinción con tinta china) o Candida spp. (7)
Autores
Dra. Marlinka Moya1, Dra. María Eugenia Galíndez2, Dr. Samuel Vega3, Dr. Rafael J. Navas G.4
1 Infectólogo pediatra. Adjunto del Servicio de Infectología pediátrica Hospital de niños J.M. de los Ríos. Pediatra Infectólogo en Centro Clínico La Urbina y Clínica Atias, Caracas.
2 Infectólogo pediatra. Adjunto del Servicio de Infectología pediátrica del Hospital Universitario de Caracas. Profesor Instructor de la Cátedra de Microbiología de la Escuela Luis Razetti UCV. Pediatra CAM de la Clínica Santiago de León, Caracas.
3 Infectólogo pediatra en Médicos sin fronteras.
4 Infectólogo pediatra. Adjunto II de la Unidad de Infectología del Servicio Autónomo Docente Hospital Central de Maracay, estado Aragua. Profesor del Departamento de Pediatría, escuela de Medicina, Universidad de Carabobo sede Aragua. Infectólogo Pediatra del Centro Médico Maracay. Doctor en Ciencias de la Educación.
BIBLIOGRAFÍA
1.- Carazo Gallego B, Cardelo Autero N, Moreno Pérez D, Gallego CB, Autero CN, Pérez MD. Meningitis. Absceso cerebral. Encefalitis aguda. Protoc diagn ter pediatr [Internet]. 2023;(2):309-28. Disponible en: www.aeped.es/protocolos/
2.-World Health Organization. WHO guidelines on meningitis diagnosis, treatment and care [Internet]. Geneva; 2025 [citado 1 de agosto de 2025]. Disponible en: https://iris.who.int/bitstream/handle/10665/381006/9789240108042-eng.pdf?sequence=1
3.- Cordero-Cabrera Y de la C, Reinoso SÁ, Pérez MS, Trujillo DH, Madrazo KP. Infections of the central nervous system in pediatric patients clinical epidemiological aspects. Salud, Ciencia y Tecnologia – Serie de Conferencias. 1 de enero de 2023;2.
4.- Khodayar-Pardo P, Llorens Córcoles AM. Infecciones del sistema nervioso central: meningitis y encefalitis. Protocolos Diagnósticos y Terapéuticos en Urgencias de Pediatría. 4.a ed. enero de 2024;
5.- Téllez González C, Reyes Domínguez S, Sanchíz Cárdenas S, Collado Caparrós JF. Meningitis bacteriana aguda. Protoc diagn ter pediatr [Internet]. 2021 [citado 24 Jul 2025];1:611-25. Disponible en: https://www.aeped.es/sites/default/files/documentos/43_meningitis_bacteriana.pdf
6.- Autore G, Bernardi L, Perrone S, Esposito S. Update on Viral Infections Involving the Central Nervous System in Pediatric Patients. [Internet]. 2021 [citado 5 de agosto de 2025];8(9):782. Disponible en: https://www.pmc.ncbi.nlm.nih.gov/articles/PMC8470393/
7.- McCarthy MW, Kalasauskas D, Petraitis V, Petraitiene R, Walsh TJ. Fungal Infections of the Central Nervous System in Children. J Pediatric Infect Dis Soc. [Internet] 2017; [citado 8 de agosto de 2025]6(3):e123-e133. Disponible en: https://www.pubmed.ncbi.nlm.nih.gov/28903523/
8.- Noor A, Kohl E. Pediatric Bacterial Meningitis: Practice Essentials, Background, Pathophysiology [Internet]. 2023 [citado 26 de julio de 2025]. Disponible en: https://emedicine.medscape.com/article/961497-overview#a2
9.-Bundy LM, Rajnik M, Noor A. Neonatal Meningitis. En: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jul 6 [citado 24 Jul 2025]. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK532264/
10.- Baddour LM, Flynn PM. Infections of cerebrospinal fluid shunts. En: Edwards MS, Tunkel AR, editores. UpToDate [Internet]. Waltham (MA): UpToDate, Inc.; 2025 Jun 2 [citado 24 Jul 2025]. Disponible en: https://www.uptodate.com/contents/infections-of-cerebrospinal-fluid-shunts/abstract/4
11.- SVPP Sociedad Venezolana de Puericultura y Pediatría. Manual de Antibióticos en Pediatría. 2ª ed. Venezuela: SVPP; 2014